第14章 筑波大学物理工学系教授(2001年11月~2018年3月):研究編
14-1. 超並列MRマイクロスコープを用いたヒト胚子標本の大量撮像
1998年に,旧知の京大の松田哲也先生から,京大の解剖学教室の塩田浩平先生をご紹介いただき,ヒト胚子標本の撮像を依頼された.当初は,研究の重要性と意義をあまり理解することができなかったが,色々なお話を聞く内に,大変重要な研究テーマであることが分かってきた.
すなわち,京都大学医学部附属先天異常標本解析センターには,1950年代から1960年代にかけて,優生保護法に従った合法的な人工妊娠中絶により収集された数万体の化学固定ヒト胚子標本が所蔵されており,その永続的な維持の困難さなどから,その非破壊的かつ三次元的な構造計測が期待されていた.また,この標本は,世界最大の化学固定ヒト胚子コレクションであるばかりでなく,倫理的な理由などにより,今後,二度と得ることができない非常に貴重なものであった.このために,これらの標本の三次元MRマイクロスコープ撮像が期待されており,そのための技術開発をスタートした.
この研究における最大の目標は,「大量撮像」ということにあったので,1997年に開発したMRmicsの手法を発展させ,大口径の超伝導磁石の中に,多数のグラジエントプローブを挿入し,同一パルスシーケンスを同時に動作させて,複数のプローブから画像を同時に取得する超並列型MRマイクロスコープを開発した.このシステムは,当初,筑波大病院の静磁場強度1.5 TのMRI装置の磁場を用い,化学固定マウスを用いてそのコンセプトを実証した(文献1).そして,その後,ヒト胚子標本の撮像には,静磁場強度2.35T,室温開口径40cmの超伝導磁石を使用した.
この方式では,水平開口の超伝導磁石を使用し,鉛直に設置した試験管に対して,静磁場方向に垂直なソレノイドRFが使用できるため,鞍型コイルに比べ3倍程度のSNR向上を実現することができるメリットも有していた.図14-1は,動物実験センターの静磁場強度2.35Tの超伝導磁石を用いた,超並列型MRマイクロスコープの全容である.グラジエントプローブは,4チャンネルと8チャンネルのものを作成し,送受信系は,8チャンネルのものを作成した.PCとグラジエント電源はすべてのチャンネルに共通のものを使用し,同一のパルスシーケンスで動作させた.
標本としては,カーネギーステージ(CS)が,13~23のものを使用し,京都大学で厳選してNMR用試験管に挿入してもらったものを輸送用トランクに入れ,100~200本単位で定期的に筑波大と京大の間を携えて輸送した.撮像したサンプルは,CS13が29体,CS14が138体,CS15が125体,CS16が126体,CS17が128体,CS18が124体,CS19が147体,CS20が141体,CS21が132体,CS22が62体,CS23が52体,合計1204体であった.その代表的な正中断面を図14-2に示す.
システムの開発と製作に約1年,実際の撮像には2年くらいを要した.システムの開発と製作には,松田善正君,拝師智之君の貢献が大きかった.また,城南電子研究所の丸谷光廣さんにもご尽力いただいた.さらに,8チャンネルのプローブの作成や,撮像した3D画像の回転と正中断面の切り出しなどに,大竹陽介君,小野真也君,半田晋也君が協力してくれた.この成果は,2007年に,日本磁気共鳴医学会のMagnetic Resonance in Medical Sciencesに公表され,その年の優秀論文賞を受賞した(図14-3)(文献2).また,この成果は,この研究に一番力を尽くした松田善正君の博士論文となった.

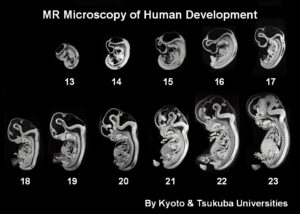
図14-1 超並列型MRマイクロスコープ 図14-2 撮像したヒト胚子標本の代表的正中断面画像

図14-3 日本磁気共鳴医学会優秀論文賞(2008年)
2.35Tの超並列型MRマイクロスコープで撮像したヒト胚子標本の画像のマトリクスサイズは,NMR信号のSNR,測定時間,コンピュータの処理能力などから,128×128×256画素であった.そこで,分解能を向上させるために,さらに高い静磁場強度を有する9.4Tの超伝導磁石を科研費で導入し,撮像システムを構築した(図14-4).このシステムでは,信号のダイナミックレンジを確保するため,高周波信号を2分割して,異なるゲインで増幅してから2チャンネルで同時にデジタルサンプリングを行った.その結果,256×256×512画素の図14-5に示すような画像を取得することができた(文献3).

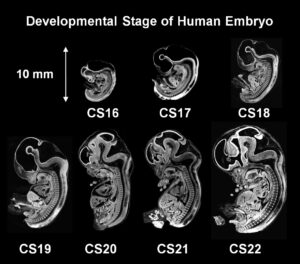
図14-4 9.4TにおけるMRマイクロスコープ 図14-5 9.4Tで撮像したヒト胚子の正中断面画像
14-2. 骨密度計測用コンパクトMRI
2000年頃に,1Tでギャップが60mmの永久磁石を製作してもらった住友特殊金属の工場を見学したところ,日立メディコ向け人体用MRIの永久磁石のプロトタイプとなる小型磁石(実物の1/4~1/5のスケール)が置いてあったのを見つけた.そして,その時,この磁石を用いた新しい応用が開けると考えて,しばらく借用した.
人体への応用を考えた場合,このような磁石が使用できるのは,サイズから言えば四肢の一部である.このような部位で,有益な診断情報が得られるものとして,骨粗鬆症診断と関節リウマチ診断を考えた.
MRIを用いた骨粗鬆症診断の基礎となる骨密度計測法としては,(1)骨髄の体積密度計測,(2)海綿骨と骨髄の磁化率差によるT2*計測,(3)海綿骨微細構造の直接計測の3種類の方法に分類される.(2)と(3)は,高磁場でないと計測ができないため,必然的に(1)の手法を採用した.また,海綿骨骨密度の計測対象領域として,橈骨,踵骨,大腿骨,脊椎骨などがあるが,磁石のサイズなどを考えて,踵骨がベストであると判断した(図14-6).なお,磁石重量の点を考えても,踵骨は計測の対象として好都合である.この磁石の静磁場強度は0.2Tであり,踵骨計測用に,改めて住友特殊金属に製作してもらったものである(重量は500kg,ギャップは160 mm).

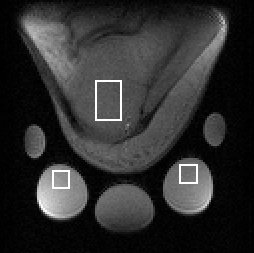
図14-6 踵骨骨密度計測用コンパクトMRI 図14-7 踵の典型的画像と評価領域
海綿骨骨密度(Trabecular Bone Volume Fraction: TBVF)を正確に計測するためには,MRI装置特有のB0分布,グラジエントの非線形性,B1分布,骨髄のT1とT2などを正確に評価する必要がある.このため,図14-7に示すようなRFプローブを作成し,各ROIにおける画素強度から,TBVFを算出する手法を開発した.
この装置を用いて,22人の筑波大学の女子学生(年齢は18~23歳:18歳は私の長女)を対象に,5週間にわたって10回の計測を行い,短期的・長期的な再現性と,超音波骨密度評価装置による音速(SOS)との相関を評価した(図14-8).また,筑波大学学園祭の時に,来学された女子学生と女性保護者を対象に計測を行い,年齢に対する有意な相関を得ることができた(図14-9).これらの結果は,Magnetic Resonance in Medicineに投稿し採択された(文献4).
学園祭における踵骨骨密度計測は,その後,筑波大の学園祭における恒例のイベントとなり,その後15年近く継続し,その後は,MRIによる小児骨年齢計測に引き継がれた.

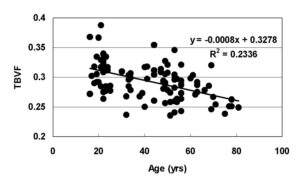
図14-8 超音波音速(SOS)とMRIによる骨密度の相関 図14-9 学園祭で計測した年齢と骨密度の相関
14-3. 骨微細構造計測用コンパクトMRI
2000年を過ぎた頃,骨形態計測の分野では,いわゆる骨量(骨密度)の評価から骨質の評価へと興味の中心が移っていった.それに伴い,Pennsylvania大学のFelix Wehrliらのグループでは,橈骨を対象として,海綿骨の骨微細構造を計測し,骨強度に対応するパラメタの評価を行っていた.彼らは,主に,1.5TのMRI装置において手首専用のRFコイルを使用して撮像を行っていた.
これに対し,私は,1.0Tの小型永久磁石(ギャップ40 mm,重量約80kg)を用いて,指骨専用のMRIを開発し,中手骨の海綿骨骨微細構造を計測することを目標とした.図14-9に示すのは,そのMRI装置(世界最小の人体用MRI)の全景である(担当:飯田奈智子さん.文献5).
この装置を用いて,長崎大学病院放射線科の伊東昌子先生のグループにお願いして,臨床データを収集していただいた.撮像条件シーケンスはTR = 50 ms,TE = 6 msの強制回復スピンエコー法,データ収集マトリクスは112×112×128,画素サイズは180 μm×180 μm×160 μm,撮像時間は11分であった.51名の健常被験者と230名の骨代謝異常疑いを有する被験者の非利き腕中指の撮像を行い,その内,46名の健常被験者と119名の患者の計測は,motion effectの影響なく撮像することができた.
図14-10は計測の典型例であり,左は22歳の健常者,右は40歳のWerner’s syndrome(早期老化症)の患者の中指の画像である.BV/TVはBone volume to total volume ratio(海綿骨体積密度),SMIはstructure model indexで海綿骨の病態を表す指標である.このように,SMIで,病態を鋭敏に評価できる可能性が示唆された.また,その後,橈骨を対象とした海綿骨骨微細構造撮像用MRIの構築にも成功した(担当:半田晋也君.文献6).

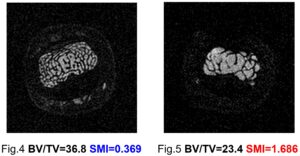
図14-9 指骨骨微細構造計測用MRI 図14-10 長崎大学病院に設置して取得した画像の例
14-4. 関節リウマチ診断用コンパクトMRI
骨粗鬆症診断用MRIと共に,臨床応用として期待されたのが関節リウマチ診断用MRIである.これは,関節リウマチの早期診断が,手のMRIで行えるという理由によるものである.ところが,多くの病院では,MRI検査は,脳神経などの重篤な病気の検査が優先されるため,検査時間枠の確保が難しく,また,実際に検査を行う場合には,手を固定する際の患者や放射線技師の負担が大きく,良好な画像を取得することが困難であった.そこで,これらの問題を解決すべく,図14-11と図14-12に示すような手専用MRIを開発した(担当:半田晋也君).


図14-11 薬事認証のためのEMC試験(東京都内某所) 図14-12 筑波大学病院における設置状況
何度かの試行錯誤の結果,このように,被験者にとって一番楽な方式である手を水平に置く方式となったが,このためには,磁石を床から高い位置に設置する必要があった.この点において,磁石メーカー(NEOMAX社)の磁気回路設計と床からの固定方法の開発が決定的であった.これにより,0.3Tの静磁場強度と均一領域(直径220 mm,厚さ80 mmの回転楕円体)を活用したシステムの構築が可能となった.また,半田晋也君の工夫などにより,シールドルームを不要とすることができた(文献7).
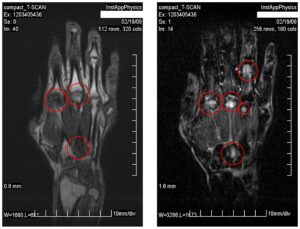

図14-13 関節リウマチ患者の症例(T1WとSTIR) 図14-14 小型MRIの入札公告
図14-13に示す画像は,この装置を用いて,筑波大学病院にて撮像した関節リウマチ患者の手の画像である.左はT1強調画像(スライス厚1.6 mm),右は脂肪抑制T2強調画像(スライス厚3.2 mm)である.患部が高信号で明瞭に描出されている.このシステムは,2008年11月に医療機器としての薬事認証を受け,2009年8月には,一般競争入札により筑波大学に納入された(図14-14).
このように,大学が一つの中心となって開発したMRI装置が,医療機器としての薬事認証を受けて商用機として発売された事例は,国内では皆無,世界でも類例のないことであった.
14-5. マウス用MRI
小型MRIの最大の応用は,マウスなどの小動物用MRIである.このためには,小型で強い磁場が発生できるヨークレス型の磁石の開発が必須であった.この目的で,住友特殊金属に作ってもらった静磁場強度1Tの3種類の磁石(ギャップは90 mm(MRTe社で購入),60 mm,40 mm(筑波大で購入し指骨海綿骨微細構造計測用のMRIに使用))を図14-15に示す.この60 mmギャップのヨークレス磁石(重量約200 kg)は,1998年に導入したコラム型の60 mmギャップの磁石(重量約1000 kg)に比べ,重量は約1/5,体積は1/10以下という驚異的な磁石であった.ギャップ90 mmの磁石を用いて構築したマウス用MRIシステムを図14-16に示す(文献8).
図14-17に,マウス頭部のプロトン密度強調画像,T1強調画像,T2強調画像の代表的スライス面を示す.いずれも3D撮像であり,FOVは25.6 mm×25.6 mm×32 mm,画像マトリクスは128×128×16,画素サイズは0.2 mm×0.2 mm×2 mmとした.研究室としては,マウスの麻酔などの経験が乏しかったが,白猪亨君と拝師智之君などの努力でクリアし,その後の製品化につながった.現在では,永久磁石を用いたマウス用MRIは,ASPECT社などいくつかの海外企業でも製品化されているが,この装置が世界初の装置である.


図14-15 三種類のサイズの1.0 Tヨークレス磁石 図14-16 マウス用MRIの全景
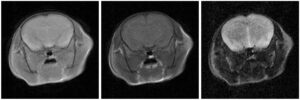
図14-17 左からプロトン密度強調画像,T1強調画像,T2強調画像.
14-6. 樹木計測用コンパクトMRI
永久磁石を用いたコンパクトMRIの大きな特長は,電源さえあれば,屋外でも使用できることである.これを実証するために,静磁場強度0.3 T,キャップ80 mm,静磁場均一領域30 mm球の永久磁石(約80 kg)を用いて,樹木計測用MRIを構築した(担当:木村武史君).図14-18に示すのは,地上から1 mくらいの位置の樹木の枝にRFコイルを巻いている様子と,RFプローブ全体をシールドしている様子である.
図14-19は,梨の枝の心材(heartwood)と辺材(sapwood)におけるADC(みかけの拡散係数:apparent diffusion coefficient)を,日射量と共に,24時間にわたって計測した結果である.このように,心材では,1日中変化がないものの,辺材では日射量に関連したとADCの変化が観測された(文献9).

図14-18 樹木計測用コンパクトMRIのRFプローブとRFシールド
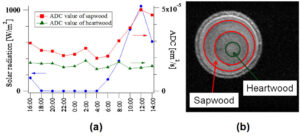
図14-19 時刻に対する日射量(左軸:青点)と梨枝における心材と辺材におけるADCの変化
この研究を,さらに発展させるために,静磁場強度0.2 T,ギャップ16 cmの永久磁石を使用し,ケヤキを研究室の傍に植えて,幹の長期的なMR撮像を行った.このシステムは,Journal of Magnetic Resonance誌(2016年)の表紙(図14-20)と,Tree Physiology誌(2020年)の表紙(図14-21)を飾ることとなった.


図14-20 Journal of Magnetic Resonanceの表紙 図14-21 Tree Physiology誌の表紙
14-7. 果実計測用コンパクトMRI
樹木内の中の流れは,MRIの応用としては興味ある研究対象であるが,果実が成長と共に,どのように内部が変化するかも,非常に興味ある研究対象である.そこで,梨果実を研究対象としている農林学系の弦間先生と瀬古澤先生にお願いして,梨果実の緩和時間とADCの経時的変化の計測を2年間にわたって行った.
図14-22は,木村武史君と下家祐人君が中心となって製作した,モバイルMRIである.このシステムは,静磁場強度0.2 T,ギャップ16 cm,静磁場均一領域10 cm球,重量200kgの永久磁石を電動台車に搭載し,さらに,磁石は上下動が可能なリフトに搭載されている.このため,図14-23に示すように,地上から1 m以上もある地点の果実の撮像が可能である.


図14-22 果実用モバイルMRI 図14-23 梨園における計測時の様子
このシステムを用いて,梨果実の直径が20 mmくらいから成熟するまでの約3か月間に亘って,ほぼ毎週,7個の梨果実のT1,T2,ADC,重量などを計測した.7個の果実は,その測定日における最大サイズのものと最小サイズのものを見出し,その間のサイズが,ほぼ等間隔になるように選択した.
図14-24は,梨重量の-1/3乗(~果実サイズの逆数)に対して,縦緩和率(1/T1)と横緩和率(1/T2)をプロットしたグラフである.なお,縦緩和は1成分であったが,横緩和は2つの成分が観測されたため,それらを分離してプロットした.このように,縦緩和率も横緩和率も,果実サイズの逆数と高い相関を示しており,核磁気緩和が細胞壁における表面緩和に起因する(Brownstein-Tarr model)ことを示している.なお,T2緩和の二つの成分に関して,遅い緩和の部分は,液胞内の水によるものであり,速い緩和の部分は,それ以外の部分によるものである.このように,果実の成長は液胞の拡大によるものであり,それが液胞内の水の表面緩和として観察されることが,本実験で明瞭に確認することができた.
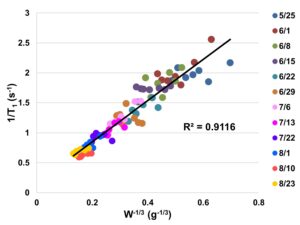
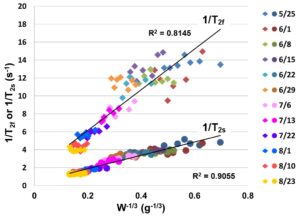
図14-24 梨重量の-1/3乗に対する縦緩和率(左)と横緩和率(右)の変化
14-8. Non Cartesian samplingによる撮像
これまで,ほぼすべての撮像では,Cartesian samplingを使用していた.それは,永久磁石を使った応用計測がメインであったことが,その理由の一つであった.いっぽう,Cartesian samplingは,さまざまなハードウェアの欠点(B0不均一性,B0不安定性,勾配磁場非線形性,渦電流効果,B1不均一性など)をカバーできるというメリットがあるが,逆にそれは,MRIの深い理解とハードウェアの改良を妨げているという面もあった.
そこで,超伝導磁石を利用する機会が増えたこともあり,Non Cartesian samplingに挑戦した.最初の例は,静磁場強度9.4 Tの縦型超伝導磁石(室温開口径54 mm)を用いたspiral samplingの実験である(担当:児玉奈緒さん.文献13).この実験では,セルフシールド型グラジエントコイルと,シールドのないグラジエントコイルを用い,まず,一定強度のグラジエントパルスに対するB0 eddy fieldを計測した(図14-25).このように,unshieldedに比べshieldedコイルを用いた方が,B0 eddy fieldはかなり小さいことが分かる.
図14-26は,spiral samplingによる画像で,左はshieldedコイルを用いた64 shotによる画像,中央は,unshieldedコイルを用いた64 shotによる画像,右は,unshieldedコイルを用いた8 shotによる画像である.画像のサイズが異なるのは,linear eddy fieldによるものである.なお,B0 eddy fieldは,MR信号の位相変化に影響するのでその補正が必要であり,linear eddy fieldは画像サイズに影響するので,その補正も必要である.
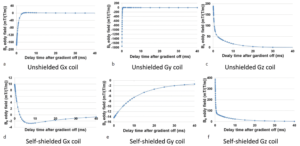
図14-25 グラジエントパルスに対するB0 eddy field.上段がunshielded,下段がshieldedコイル.

図14-26 Spiral samplingによる画像.本来のサイズは,縦横共に75 pixelである.
次に,静磁場強度1.5Tの水平開口超伝導磁石(室温開口径280 mm)を用いた3D Conesの実験を行った(担当:瀬戸井綾菜さん.文献14).3D Conesのトラジェクトリを図14-27に示す.3D Conesの長所は,radial法と同様に,エコー時間が短い撮像が可能であることと,radial法に比べサンプリング効率が良いことである.図14-28に示すように,エコー時間の短縮に限界のあるCartesian samplingであるグラジエントエコー法に比べ,T2が短い組織の描出に優れている.ただし,渦電流効果や静磁場不均一性の影響の克服が課題である.
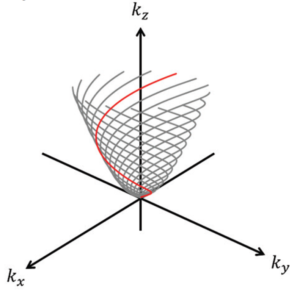
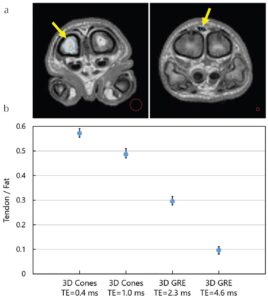
図14-27 3D Conesのトラジェクトリ 図14-28 豚足試料におけるシーケンスによる信号変化(腱/脂肪)
14-9. GPUを用いたMRI simulatorの開発
停年の3年4カ月前に,「超高速シミュレータを搭載した ユニバーサルMRIプラットフォームの開発」というJSTプロジェクト(リーダー:拝師智之)にサブリーダーとして参画し,GPUを用いたMRI simulatorの開発を行った(担当:巨瀬亮一,文献15,16).
このMRI simulator(BlochSolver)の特長は,(1)GPUに最適化されていて,それまでに公表されていたものよりも遥かに高速,(2)実験装置と同一のパルスシーケンスが動作するため実験との比較が容易,(3)サブボクセルという概念を用いることにより,高速イメージングやマルチスライスなどのシミュレーションが容易,というものである.
図14-29は,TR=20ms,TE=6ms,FA=30°,画像マトリクス数256×256×32のRF spoiled gradient echo法をシミュレーションしたもので,信号読出し方向のサブボクセル数による画像の変化を示している.このように,正しいシミュレーションを行うには,多くのサブボクセル数が必要であることが分かる.
図14-30と14-31は,励起周波数が-40kHzから+40kHzまで,8kHz間隔でグラジエントエコー・マルチスライスのシミュレーションを実施した結果であり,それぞれ,選択励起パルス(sincx)の分割点数を100点,200点とした場合の画像である.このように,分割点数が不十分な場合には,エリアジング効果が生じ,アーチファクトが発生することが示された.
このように,BlochSolverは,実用的なパルスシーケンスをシミュレーションで再現するための,有用なツールとなることを実証することができた.

図14-29 信号読出し方向のサブボクセルを増やした時の画像の変化

図14-30 マルチスライスのシミュレーション画像.選択励起パルスの分割点数が100点のときにゴーストが出現する.

図14-31 マルチスライスのシミュレーション画像.選択励起パルスの分割点数が200点ではゴーストが消失する.
- Y. Matsuda, S. Utsuzawa, T. Kurimoto, T. Haishi, Y. Yamazaki, K. Kose, I. Anno, M. Marutani. Super-parallel MR microscope. Magn Reson Med 50, 183-189 (2003)
- Y. Matsuda, S. Ono, Y. Otake, S. Handa, K. Kose, T. Haishi, S. Yamada, C. Uwabe, K. Shiota. Imaging of a Large Collection of Human Embryo Using a super-Parallel MR Microscope. Magnetic Resonance in Medical Sciences 6, 139-146 (2007)
- Y. Otake, S. Handa, K. Kose, K. Shiota, S. Yamada, C. Uwabe. Magnetic Resonance Microscopy of Chemically Fixed Human Embryos at High Spatial Resolution. Magnetic Resonance in Medical Sciences 14(2), 153-158 (2015)
- K. Kose, Y. Matsuda, T. Kurimoto, S. Hashimoto, Y. Yamazaki, T. Haishi, S. Utsuzawa, H. Yoshioka, S. Okada, M. Aoki, T. Tsuzaki. Development of a compact MRI system for trabecular bone volume fraction measurements. Magn Reson Med 52, 440-444 (2004)
- N. Iita, S. Handa, S. Tomiha, K. Kose. Development of a compact MRI for measurement of trabecular bone microstructure of the finger. Magn Res Med 57, 272-277 (2007)
- S. Handa, S. Tomiha, T. Haishi, K. Kose. Development of a compact MRI system for trabecular bone microstructure measurements of the distal radius. Magn Reson Med 58, 225-229 (2007)
- S. Handa, T. Haishi, K. Kose. Development of a local electromagnetic shielding for an extremity magnetic resonance imaging system. Rev. Sci. Instrum 79, 113706 (2008)
- Shirai, T. Haishi, S. Utsuzawa, Y. Matsuda, K. Kose .Development of a compact mouse MRI using a yokeless permanent magnet. Magnetic Resonance in Medical Sciences 4, 137-143 (2005)
- T. Kimura, Y. Geya, Y. Terada, K. Kose, T. Haishi, H. Gemma, Y. Sekozawa. Development of a mobile magnetic resonance imaging system for outdoor tree measurements. Rev. Sci. Instrum 82, 053704 (2011)
- A. Nagata, K. Kose, Y. Terada. Development of an outdoor MRI system for measuring flow in a living tree. J Magn Reson 265, 129-138 (2016)
- Y. Terada, Y. Horikawa, A. Nagata, K. Kose, K. Fukuda. Dynamics of xylem and phloem sap flow in an outdoor zelkova tree visualized by magnetic resonance imaging. Tree Physiology, 40, 290-304 (2020)
- Y. Geya, T. Kimura, H. Fujisaki, Y. Terada, K. Kose, T. Haishi, H. Gemma, Y. Sekozawa. Longitudinal NMR parameter measurements of Japanese pear fruit during the growing process using a mobile magnetic resonance imaging system. J Magn Reson 226, 45-51 (2013)
- N. Kodama, A. Setoi, K. Kose. Spiral MRI on a 9.4T Vertical-bore Superconducting Magnet Using Unshielded and Self-shielded Gradient Coils. Magnetic Resonance in Medical Sciences 17, 174-183 (2018)
- A. Setoi, K. Kose. 3D Cones Acquisition for Human Extremities Using a 1.5T Superconducting Magnet and an Unshielded Gradient Coil Set. Magn Reson Med Sci 18, 88–95 (2019).
- R. Kose, K. Kose. BlochSolver : A GPU-optimized fast 3D MRI simulator for experimentally compatible pulse sequences. J Magn Reson 281, 51–65 (2017)
- R. Kose, A. Setoi, K. Kose. A fast GPU-optimized 3D MRI simulator for arbitrary k-space sampling. Magn Reson Med Sci 18, 208-218 (2019)
